La EMA explicó que el comité de medicamentos de uso humano llevará a cabo una “evaluación acelerada de los datos presentados por la empresa que comercializa dicha vacuna, incluidos los datos de un “gran ensayo clínico en adolescentes” de más de 12 años que demostró que la vacuna tiene una eficacia del 100 % en este grupo de edad
Agencias
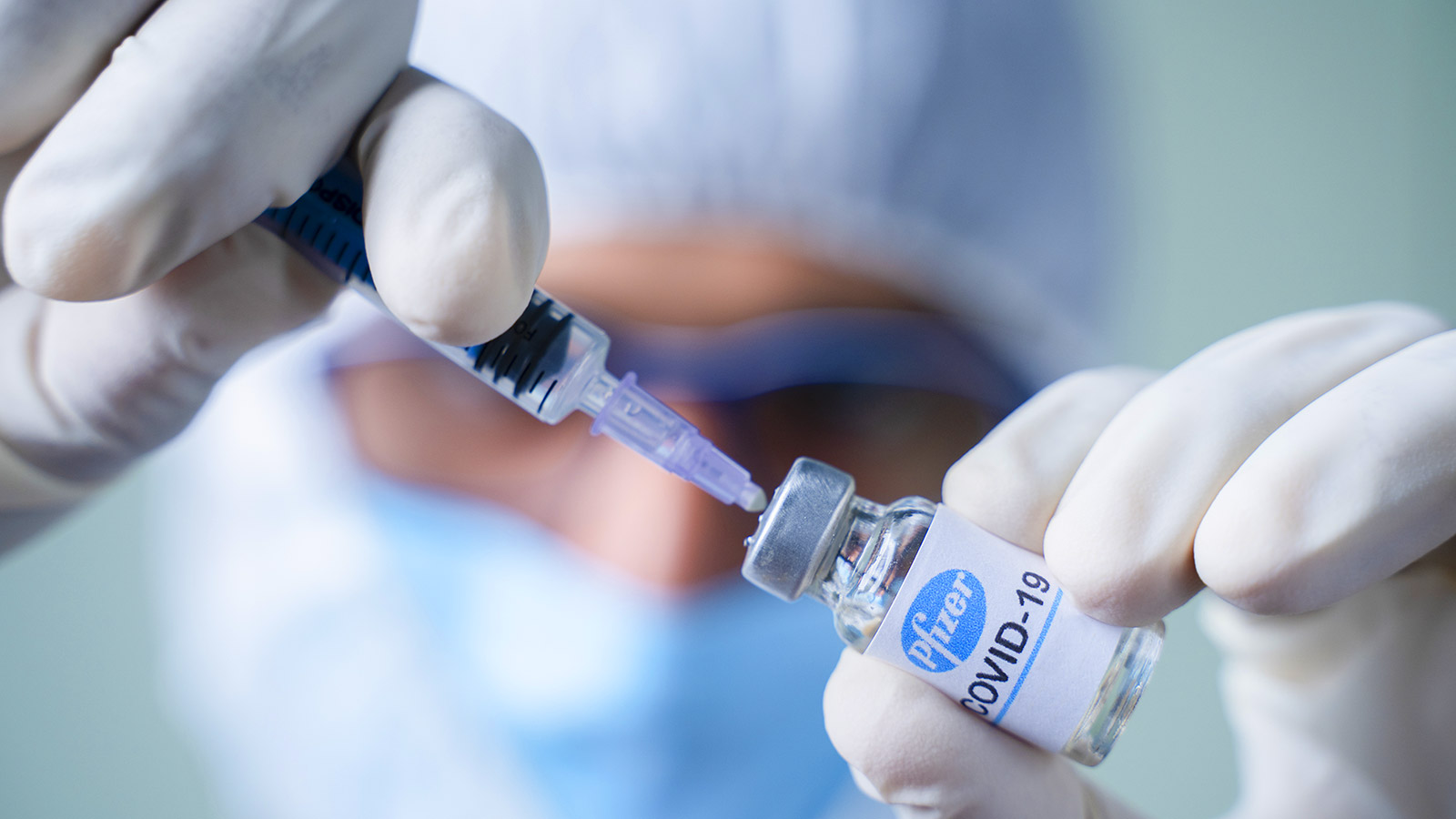
03 Mayo 2021, Ámsterdam. – Este lunes la Agencia Europea del Medicamento comenzó con la evaluación de la solicitud de las farmacéuticas Pfizer y BioNTech para incluir a los menores de entre 12 y 15 años en la vacunación con su preparado contra Covid-19, y espera comunicar el resultado de la evaluación en el mes de junio.
Ante esto la agencia, con sede en Ámsterdam, explicó que el comité de medicamentos de uso humano llevará a cabo una “evaluación acelerada de los datos presentados por la empresa que comercializa dicha vacuna, incluidos los datos de un “gran ensayo clínico en adolescentes” de más de 12 años que demostró que la vacuna tiene una eficacia del 100 % en este grupo de edad.
Luego de esto la EMA deberá determinar si los criterios de seguridad y eficacia se mantienen para el nuevo grupo de edad entre los 12 y 15 años, antes de decidir si recomendar la extensión de la indicación a ese grupo de edad.
Por lo que dicha agencia espera comunicar el resultado de su evaluación para junio, a menos que se necesite información adicional que pueda retrasar el proceso de análisis, y el CHMP enviará entonces a la Comisión Europea sus conclusiones para que emita una decisión final legalmente vinculante aplicable a todos los Estados miembros de la Unión Europea.
Es importante mencionar que de lograr el respaldo de la Agencia europea del medicamento, esta sería la primera vacuna que consigue una autorización en esta región para su uso en menores de 16 años.